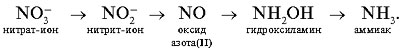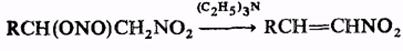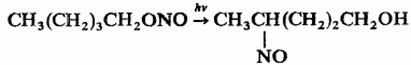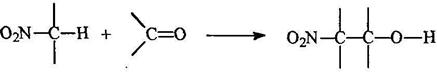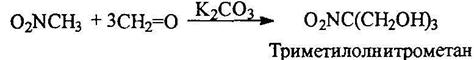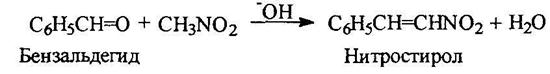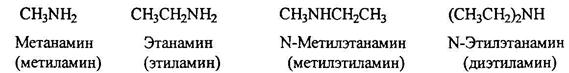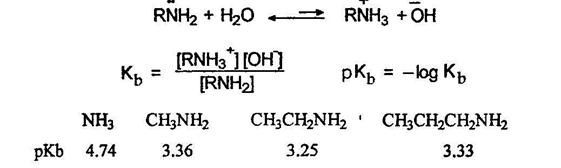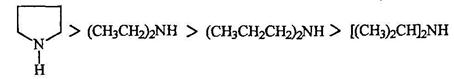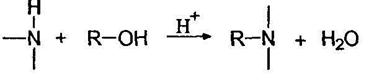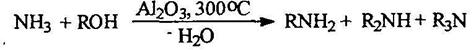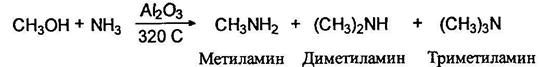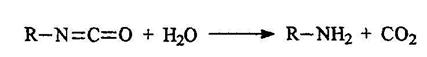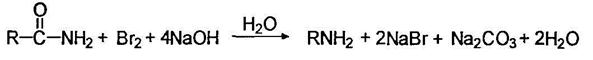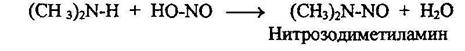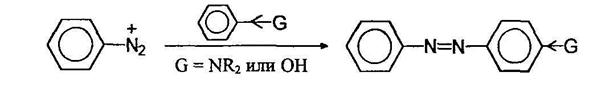|
Курсовая работа: Синтез и свойства амилнитритаКурсовая работа: Синтез и свойства амилнитритаФедеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Самарский государственный технический университет Кафедра: «Органическая химия» АМИЛОВЫЙ ЭФИР АЗОТИСТОЙ КИСЛОТЫ Выполнил: Руководитель: Самара, 2007 г. Содержание Введение Общие сведения Практическое применение Амилнитрит, как противоядие при отравлениях Проблема нитратов и нитритов Методика синтеза Литературный обзор. Неорганические нитриты Органические нитриты Нитросоединения Способы получения нитросоединений Реакции нитросоединений Амины Основность аминов Методы получения Реакции аминов Диазо- и азосоединения Реакции солей арилдиазония Выводы Список литературы Общие сведенияАмилнитрит C5H11NO2 (изоамиловый эфир азотистой кислоты). Молекулярная масса (в а. е. м.): 117,15. Температура кипения (в °C): 104. Прозрачная желтоватая, легкоподвижная, весьма летучая жидкость фруктового запаха. Легко воспламеняется. Очень мало растворим в воде; смешивается во всех соотношениях со спиртом, эфиром, хлороформом. Плотность 0,8528 (20°C, г/см3). Практическое применениеАмилнитрит, как противоядие при отравленияхАмилнитрит является основным представителем органических нитритов. Еще в конце 60-х годов прошлого века было обнаружено свойство этого соединения вызывать при вдыхании паров расширение кровеносных сосудов и купировать приступы грудной жабы (стенокардии). Уже в те годы было рекомендовано больным грудной жабой смачивать кусочек ткани несколькими каплями (5 – 10) амилнитрита и вдыхать его пары. Препарат начинал действовать через 30 - 60 с. Одновременно с прекращением загрудинных болей отмечалось покраснение лица и развивалась головная боль (в связи с расширением сосудов мозга). С появлением нитроглицерина и обнаружением его эффективности при стенокардии, амилнитрит в связи с выраженными побочными явлениями и кратковременностью действия, стали назначать реже. В настоящее время амилнитрит как антиангинальное средство практически не применяется. Лишь в исключительных случаях, при отсутствии других антиангинальных средств, он может быть временно использован для купирования приступов стенокардии. Вместе с тем амилнитрит, нашел применение как противоядие при отравлении синильной кислотой и ее солями, что объясняется способностью амилнитрита (и других нитритов) образовывать в крови метгемоглобин, связывающий ион СN, и предупреждать этим поражения тканевых дыхательных ферментов. Применяют амилнитрит путем вдыхания после нанесения его на носовой платок, небольшой кусок ваты или марли. Назначают взрослым по 2 - 3 капли, детям (старше 5 лет) - по 1 – 2 капли. Высшие дозы для взрослых (для вдыхания): разовая 0,1 мл (6 капель); суточная 0,5 мл (30 капель). При отравлениях цианидами его применяют повторно в указанных выше дозах (до общей дозы 0,5 – 1 мл). Противопоказания такие же, как для нитроглицерина. Форма выпуска: в обычных ампулах и в ампулах с ватно-марлевой оплеткой (по 0,5 мл). Вскрытие ампул сопровождается легким взрывом в связи с давлением паров, образующихся в ампуле при хранении и нагревании. Пары амилнитрита образуют с воздухом взрывоопасные смеси. Хранение: список Б. В запаянных ампулах в прохладном, защищенном от света месте. Проблема нитратов и нитритовПроблема нитратов активно обсуждается общественностью нашей страны. Попробуем разобраться в этом вопросе и мы. Нитраты – соли азотной кислоты, например NaNO3, KNO3, NH4 NO3, Mg(NO3)2. Они являются нормальными продуктами обмена азотистых веществ любого живого организма – растительного и животного, поэтому «безнитратных» продуктов в природе не бывает. Даже в организме человека в сутки образуется и используется в обменных процессах 100 мг и более нитратов. Из нитратов, ежедневно попадающих в организм взрослого человека, 70% поступает с овощами, 20% – с водой и 6% – с мясом и консервированными продуктами. При потреблении в повышенных количествах нитраты в пищеварительном тракте частично восстанавливаются до нитритов (более токсичных соединений), а последние при поступлении в кровь могут вызвать метгемоглобинемию. Кроме того, из нитритов в присутствии аминов могут образоваться N-нитрозамины, обладающие канцерогенной активностью (способствуют образованию раковых опухолей). При приеме высоких доз нитратов с питьевой водой или продуктами через 4–6 ч появляются тошнота, одышка, посинение кожных покровов и слизистых, понос. Сопровождается все это общей слабостью, головокружением, болями в затылочной области, сердцебиением. Первая помощь обильное промывание желудка, прием активированного угля, солевых слабительных, свежий воздух. Безопасная доля нитратов, допустимая суточная доза нитратов для взрослого человека составляет 325 мг в сутки. Как известно, в питьевой воде допускается присутствие нитратов до 45 мг/л. Рекомендуемое потребление продуктов питания, где используется питьевая вода (чай, первые и третьи блюда), примерно 1,0–1,5 л, максимум – 2,0 л в день. Таким образом, с водой взрослый человек может употребить около 68 мг нитратов. Следовательно, на пищевые продукты остается 257 мг нитратов. Исследования показали, что токсическое действие нитратов пищевых продуктов проявляется слабее, чем содержащихся в питьевой воде, примерно в 1,25 раза. Фактически безопасно с пищевыми продуктами потреблять 320 мг нитратов в сутки. Для овощей и фруктов установлены следующие значения предельно допустимых концентраций нитратов. Предельно допустимые концентрации нитратов продуктах растениеводства
Основные источники пищевых нитратов – практически это исключительно растительные продукты. В животных продуктах (мясо, молоко) содержание нитратов весьма незначительно. Максимальное накопление нитратов происходит в период наибольшей активности растений при созревании плодов. Чаще всего максимальное содержание нитратов в растениях бывает перед началом уборки урожая. Поэтому недозрелые овощи (кабачки, баклажаны) и картофель, а также овощи раннего созревания могут содержать нитратов больше, чем достигшие нормальной уборочной зрелости. Кроме того, содержание нитратов в овощах может резко увеличиться при неправильном применении азотистых удобрений (не только минеральных, но и органических). Например, при внесении их незадолго до уборки. Определение нитритов в растениях Оборудование и реактивы.
Лезвие, пипетка, дифениламин (кристаллический), серная кислота (конц.), раствор
стрептоцида (таблетку 0,5 г растворить в 50 мл аптечной соляной
кислоты), раствор антипирина (одну таблетку растворить в 50 мл аптечной
соляной кислоты).
Образующийся аммиак взаимодействует с органическими кислотами, в результате получаются аминокислоты: NH3 + органическая
кислота Однако избыточное количество нитратов не восстанавливается и, попадая в организм человека, оказывает неблагоприятное воздействие на него. При попадании в желудочно-кишечный тракт человека нитраты превращаются в нитриты, которые вызывают отравление организма: появляется головокружение, снижается работоспособность, увеличивается содержание в крови молочной кислоты, холестерина, белков, блокируется гемоглобин, т.к. нитриты могут вступать во взаимодействие с ним, образуя метгемоглобин. В результате нарушается тканевое дыхание. При больших дозах развивается «синюха» и наступает смерть. Для проведения качественной пробы на присутствие нитритов в растениях на поверхность свежего среза наносят несколько кристалликов дифениламина и смачивают их двумя каплями концентрированной серной кислоты. Интенсивное синее окрашивание среза указывает на наличие большого количества нитритов, розовое на небольшое их содержание и отсутствие окрашивания – на отсутствие нитритов или на очень незначительное их содержание. Для определения нитритов и нитратов можно воспользоваться доступными аптечными препаратами: антипирином (пирамидон) и стрептоцидом, которые выполняют функцию восстановителя, при этом появляется характерное окрашивание. Для исследования были взяты овощи, выращенные на собственном земельном участке и купленные в магазине. Обнаружено, что томаты, бананы, груши и огурцы не содержат нитратов и нитритов. Персики, капуста, редис, перец, яблоки содержали небольшое количество нитритов. А баклажаны, морковь и апельсины содержали очень большое количество нитритов. Значит, употреблять их в пищу нежелательно. Если в продукции присутствует избыток нитритов, зелень – петрушку, укроп, салат и другое – необходимо поставить, как букет, в воду на прямой солнечный свет. В таких условиях нитраты в листьях в течение 2–3 ч полностью перерабатываются и потом практические не обнаруживаются. После этого зелень можно без опасений употреблять в пищу. Свеклу, кабачки, капусту, тыкву и другие овощи перед приготовлением необходимо нарезать мелкими кубиками и 2–3 раза залить теплой водой, выдерживая по 5–10 мин. Нитраты хорошо растворимы в воде, особенно теплой, и вымываются из овощей. Варка овощей снижает содержание нитратов на 50 и даже 80%. Квашение, соление, маринование также уменьшают содержание нитратов в овощах. А вот сушка, приготовление соков и пюре, наоборот, повышают концентрацию нитратов. Владение информацией о накапливании нитратов в растениях и о превращении нитратов в нитриты и N-нитрозамины поможет вам правильно питаться и сохранить свое здоровье. Методика синтеза
Реактивы: амиловый спирт 77 г, нитрит натрия 38 г, серная кислота концентрированная 25 г, бикарбонат натрия 1 г, сульфат натрий, безводный 1 г, хлористый натрий. Аппаратура. Колба круглодонная, трехгорлая емк. 500 мл. Воронка капельная. Воронка Бюхнера. Прибор для перегонки в вакууме. Мешалка. В круглодонную трехгорлую колбу, снабженную мешалкой, капельной воронкой и термометром, достигающим почти до дна колбы, помещенную в охладительную смесь, вливают раствор 38 г (0,55 моля) нитрита натрия в 150 мл воды. Когда температура раствора понизится до 0°, к нему по каплям приливают смесь 15 мл воды, 25 г (0,5 моля) концентрированной серной кислоты и 77 г (0,5 моля) амилового спирта. Колебания температуры не должны превышать ± 1°, приливание смеси к раствору нитрита длится около 2 часов. После 15-часового стояния отфильтровывают выделившийся осадок сульфата натрия, в делительной воронке отделяют слегка желтоватый слой амилнитрита от воды (примечание 1), промывают его раствором бикарбоната натрия, раствором хлористого натрия, сушат безводным сульфатом натрия и перегоняют в вакууме: т. кип. 29°/40 мм рт. ст., 104°/760 мм рт. ст. Выход – 45 г (80% от теоретического). Примечание Вдыхание паров амилнитрита вызывает головные боли и боли в сердце. Его следует хранить в сухом и холодном месте не более двух недель с момента получения. Продукты разложения амилнитрита содержат воду, окислы азота, амиловый спирт и полимеры валерианового альдегида Литературный обзор. Неорганические нитритыНеорганические нитриты, соли азотистой кислоты HNO2. Используют прежде всего нитриты щелочных металлов и аммония, меньше – щелочно-земельных и Зd-металлов, Рb и Ag. О нитритах остальных металлов имеются только отрывочные сведения. Нитриты металлов в степени окисления +2 образуют кристаллогидраты с одной, двумя или четырьмя молекулами воды. Нитриты образуют двойные и тройные соли, напр. CsNO2xAgNO3 или Ba(NO2)2•Ni(NO2)2•2KNO3, а также комплексные соединения, например Na3[Co(NO2)6]. Кристаллические структуры известны лишь для нескольких безводных нитритов. Анион NО2-- имеет нелинейную конфигурацию; угол ONO 115°, длина связи N—О 0,115 нм; тип связи М—NО2 ионно-ковалентный. СВОЙСТВА НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ НИТРИТОВ Показатель KNO2 AgNO2 Ca(NO2)2 Ba(NO2)2 Сингония Моноклинная Ромбическая Кубическая Гексагональная Темп. пл., °С 440 120 220 277 (с разд.) (с разл.) Р-римость в воде,г в 100 г 306,7 0,41 84,5 67,5 (20°С) (25°С) (18°С) (20°С) Хорошо растворимы в воде нитриты К, Na, Ва, плохо – нитриты Ag, Hg, Сu. С повышением температуры растворимость нитритов увеличивается. Почти все нитриты плохо растворимы в спиртах, эфирах и малополярных растворителях. Нитриты термически малоустойчивы; плавятся без разложения только нитриты щелочных металлов, нитриты остальных металлов разлагаются при 25-300°С. Механизм разложения нитриты сложен и включает ряд параллельно-последовательных реакций. Основные газообразные продукты разложения – NO, NO2, N2 и О2, твердые – оксид металла или элементный металл. Выделение большого количества газов обусловливает взрывное разложение некоторых нитритов, например NH4NO2, который разлагается на N2 и Н2О. Характерные особенности нитритов связаны с их термической нестойкостью и способностью нитрит-иона быть как окислителем, так и восстановителем, в зависимости от среды и природы реагентов. В нейтральной среде нитриты обычно восстанавливаются до NO, в кислой окисляются до нитратов. Кислород и СО2 не взаимодействуют с твердыми нитритами и их водными растворами. Нитриты способствуют разложению азотсодержащих органических веществ, в частности аминов, амидов и др. С органическими галогенидами RX нитриты реагируют с образованием как нитритов RONO, так и нитросоединений RNO2. Промышленное получение нитритов основано на абсорбции нитрозного газа (смеси NO + NO2) растворами Na2CO3 или NaOH с послед, кристаллизацией NaNO2; нитриты остальных металлов в промышленности и лабораториях получают обменной реакцией солей металлов с NaNO2 или восстановлением нитратов этих металлов. Анализ нитритов на нитрит-ион основан на его восстановлении сплавом Деварда (50% Сu, 45% А1, 5% Zn) до NH3 и поглощении NH3 титрованными растворами кислот. Нитриты применяют для синтеза азокрасителей, в производстве капролактама, в качестве окислителей и восстановителей в резинотехнике, текстильной и металлообрабатывающей промышленности, как консерванты пищевых продуктов. Нитриты, например NaNO2 и KNO2, токсичны, вызывают головную боль, рвоту, угнетают дыхание и т.д. При отравлении NaNO2 в крови образуется метгемоглобин, повреждаются мембраны эритроцитов. Возможно образование нитрозаминов из NaNO2 и аминов непосредственно в желудочно-кишечном тракте. Органические нитритыОрганические нитриты, эфиры азотистой кислоты HNO2. Содержат одну или несколько групп О—N=O, связанных ковалентной связью с атомом углерода органического радикала. Низшие алкилнитриты – газы, остальные – бесцветные или желтоватые жидкости, не растворимые в воде, смешиваются с обычными органическими растворителями. Органические нитриты более летучи, чем изомерные им нитросоединения. Физические свойства некоторых органические нитритов приведены в таблице. СВОЙСТВА НЕКОТОРЫХ ОРГАНИЧЕСКИХ НИТРИТОВ Соединение Т.кип,
°С Метилнитрит CH3ONO - 12 0,991 Пропилнитрит C3H7ONO 48,5 0,935 1,3604 Бутилнитрит C4H9ONO 77,8 0,8823 1,3768 Изобутилнитрит C4H9ONO 67 0,8699 1,3715 Изопентилнитрит (изоамил- нитрит) (CH3)2CHCH3CH2ONO 99,2 0,8828 1,3918 Вращение вокруг связи О—N заметно заторможено (барьер вращения ∆G* 34 кДж/моль), поэтому s-циc- и s-транс-конформеры спектрально различимы. ИК спектр органических нитритов имеет характеристические полосы 1613-1625 и 1653-1681 см-1 (N=O) соотв. для s-цис- и s-транс-форм. При комнатной температуре органические нитриты медленно разлагаются, на свету низшие органические нитриты могут взрываться. В кислой среде легко гидролизуются; это позволяет использовать органические нитриты в качестве мягких нитрозирующих агентов (для получения малостабильных солей диазония, дезаминирования алкиламинов, нитрозирования фенолов и СН-кислот и т.п.). Органические нитриты, имеющие активированный атом Н при β-углеродном атоме, могут отщеплять HNO2, например:
При действии N2O5 органические нитриты окисляются в нитраты, при действии гидразина или LiAlH4 восстанавливаются в соответствующие спирты. Органических нитриты, содержащие в молекуле более трех атомов С, претерпевают фотохимическую перегруппировку в нитрозосоединения (Бартона реакция), напр.:
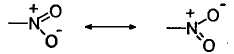
Реакция идет стереоселективно и используется для введения функциональных групп в неактивные участки сложных молекул, например, стероидов. Получают органические нитриты взаимодействием спиртов с различными нитрозирующими агентами [NaNO2/H2SO4, NaNO2/Al2(SO4)3, оксиды азота, NOCl/пиридин, NOBF4] или взаимодействием алкилгалогенидов с солями HNO2 (наряду с нитросоединениями). Органические нитриты высокотоксичные соединения. Этил- и пентилнитриты учащают пульс, понижают кровяное давление, окисляют гемоглобин в метгемоглобин. Органических нитриты обладают сосудорасширяющим и спазмолитическим действием. Изопентилнитрит - противоядие при отравлении синильной кислотой и ее солями. Органические нитриты – полупродукты в органическом синтезе. НитросоединенияНитросоединениями называют производные углеводородов, в которых один или несколько атомов водорода замещены на нитрогруппу -NO2. В зависимости от углеводородного радикала, к которому присоединена нитрогруппа, нитросоединения делятся на ароматические и алифатические. Алифатические соединения различают как первичные 1°, вторичные 2 ° и третичные 3°, в зависимости от того к 1 °, 2 ° или 3° атому углерода присоединена нитрогруппа. Нитрогруппу не следует путать с нитритной группой -ONO. Нитрогруппа имеет следующее строение:
Наличие полного положительного заряда на атоме азота обусловливает наличие у нее сильного -1-эффекта. Наряду с сильным -1-эффектом нитрогруппа обладает сильным -М-эффектом. Способы получения нитросоединенийНитрование углеводородов.
Ароматические нитросоединения получают, как правило, прямым нитрованием аренов и ароматических гетероциклических соединений. Нитрометан также может быть получен нитрованием метана. Синтез нитросоединений из галогенуглеводородов
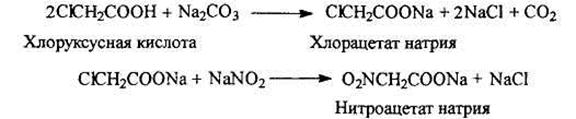
Синтез нитрометана из хлоруксусной кислоты Нитрометан обычно получают из хлоруксусной кислоты по следующей схеме:
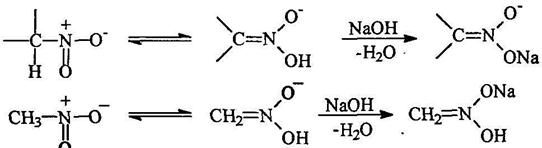
Реакции нитросоединенийТаутомерия алифатических нитросоединений
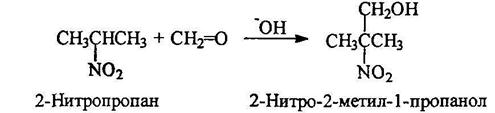
Конденсация алифатических нитросоединений с альдегидами
Практическое значение имеет триметилолнитрометан, получаемый из нитрометана и формальдегида:
Ароматические нитросоальдегиды конденсируются с нитрометаном с отщеплением воды:
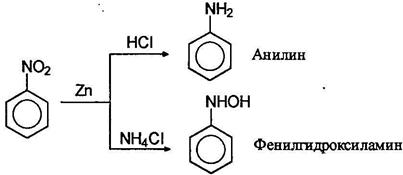
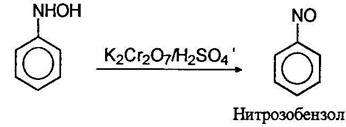
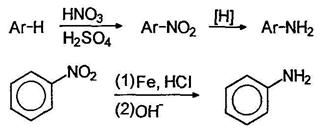
Восстановление нитросоединений. Важнейшее практическое значение имеют реакции восстановления нитрогруппы в нитроаренах. В зависимости от рН среды и используемого восстановителя могут быть получены различные продукты. В нейтральной и щелочной среде активность обычных восстанавливающих агентов по отношению к нитро соединениям меньше, чем в кислой среде. Характерным примером может служить восстановление нитробензола цинком. В избытке соляной кислоты цинк восстанавливает нитробензол в анилин, в то время как в буферном растворе аммонийхлорида - в фенилгидроксиламин:
Фенилгидроксиламин далее может быть окислен до нитрозобензола:
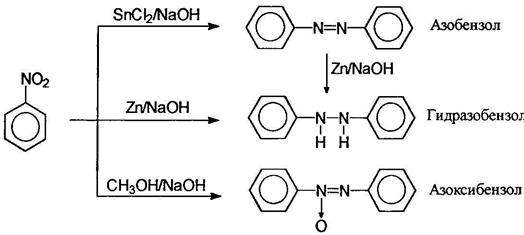
Восстановлением нитробензола хлоридом олова (II) получают азобензол, а цинком в щелочной среде - гидразобензол; восстановлением спиртом в щелочной среде можно получить азоксибензол:
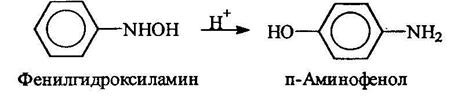
Азоксибензол получают обработкой нитробензола раствором щелочи в метаноле, при этом метанол окисляется в муравьиную кислоту. В кислой среде арилгидроксиламины подвергаются перегруппировке:
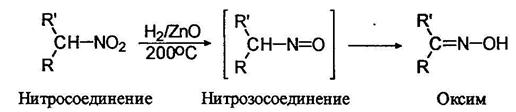
Известны методы неполного восстановления и нитроалканов:
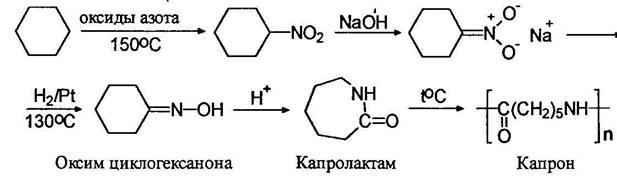
На этом основан один из промышленных методов получения капрона. Нитрованием циклогексана получают нитроциклогексан, который восстановлением переводят в оксим циклогексанона и далее с помощью перегруппировки Бекмана – в капролактам и полиамид – исходное вещество для приготовления волокна – капрона:
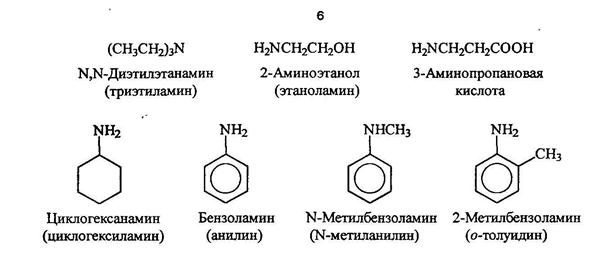
АминыПо систематической номенклатуре амины называют путем добавления приставки амин к названию углеводорода. По рациоальной номенклатуре их рассматривают как алкил или ариламины.
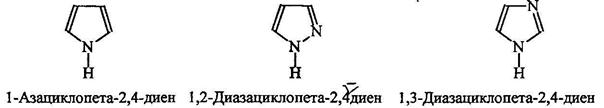
Гетероциклические амиы называют по соответствующему углеводороду вставляя приставку аза-, диаза- или триаза для обозачения количества атомов азота.
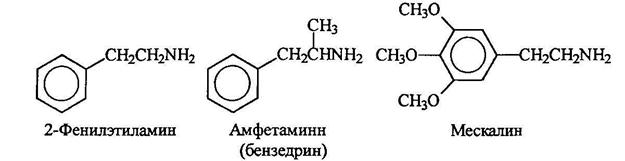
Аминами являются многие биологически активные соединения, обладающие, например, физиологическим и психологическим действием. Некоторые из них являются производными 2-фенилэтиламинна. Амфетамин является мощным стимулятором. Мескалин является галюциногеном.
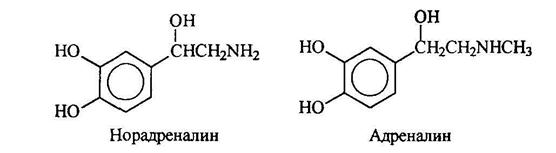
Адреналин и норадреналин являются гормонами, поступающими в кровь, когда животные ощущают опасность. Адреналин вызывает повышение кровяного давления, учащение пульса и расширение подходов к легким. Норадреналин также повышает кровяное давление. Он участвует в передаче импульса от ондого конца нервного волокна к другому.
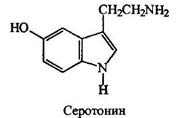
Серотонин поддерживает нормальный уровень умственной деятельности. Предполагается, что шизофрения связана с нарушением метаболизма серотонина.
Основность аминовАммиак и амины благодаря наличию на их атомах азота неподеленной пары электронов обладают нуклеофильными свойствами, т.е. предоставляют эту пару обедненному электронами атому углерода. Они способны предоставлять ее и протону, т.е. обладать основностью. Все простейшие алифатические амины взаимодействуя с водой генерируют гидроксид-анион и, следовательно, окрашивают лакмус в синий цвет:
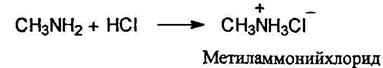
Подобно аммиаку амины при действии минеральных кислот превращаются в соли: Основные свойства аминов обусловлены способностью свободных (неподеленных) электронов атомов азота присоединять протон.
Основность аминов тем выше, чем больше электронная плотность на атоме азота (чем выше электронодонорный характер атома азота). Алифатические амины - более сильные основания, чем аммиак, поскольку алкильные группы обладают +1-эффектом. Их основность последовательно возрастает при переходе от первичных аминов ко вторичным, но несколько падает при переходе к третичным. Нуклеофильность и основность аминов изменяются, как правило, симбатно: они уменьшаются с уменьшением электроннной плотности на атоме азота или при его пространственном экранировании и увеличиваются с увеличением электронной плотности на атоме азота или с увеличением его доступности. В качестве примера можно привестиосновность метиламинов. По силе основности они располагаются в следующий ряд:
Влияние пространственного фактора на основность и на нуклеофильность аминов наглядно демонстрируется сравнением свойств некоторых вторичных аминов.
Анилин и другие ароматические амины являются слабыми основаниями. В отличие от алифатических аминов они не окрашивают водные растворы лакмуса в синий цвет, т.е. не генерируют гидроксид-анион при взаимодействии с водой. Анилин не образует солей с такими слабыми кислотами, как угольная, синильная, сероводород и др. Гидрохлорид анилина гидролизуется в воде, а сульфат анилина в воде не растворим. 2.2. Методы полученияВосстановление нитросоединений Восстановление ароматических нитросоединений в сочетании с нитрованием аренов является главным способом получения аминов.
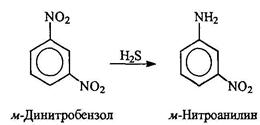
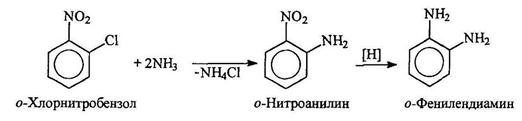
Использование в качестве восстановителя сероводорода позволяет восстанавливать одну из нитрогрупп в динитроаренах:
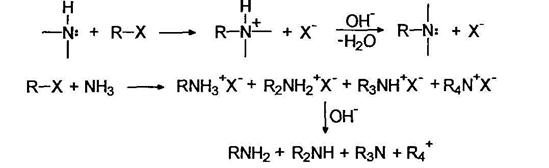
Аммонолиз галогенуглеводородов Наиболее очевидный путь
синтеза аминов заключается в алкилировании аммиака или амина алкилгалогенидами.
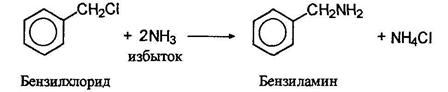
Однако, при проведении этой реакции возможно многократное алкилирование: Недостатком этой реакции является то, что ее трудно остановить на какой-либо стадии. Первичные амины все же можно получать при использовании большого избытка аммиака, например:
Ароматические амины тоже можно получать из арилхлоридов и аммиака, но для этого требуются очень жесткие условия. Однако, если в орто- и пара-положениях к хлору находятся такие сильно электроноакцепторные группы, как нитрогруппа, замещение происходит сравнительно легко, например:
Алкилирование аммиака и аминов спиртами. Так получают метиламины:
В промышленности алкилирование аммиака проводится первичными спиртами в присутствии хромита меди или окиси алюминия и других катализаторов при ЗОО°С. При этом образуется смесь аминов, которую далее разделяют ректификацией:
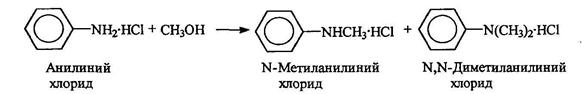
Алкилирование анилина обычно ведется спиртами в присутствии кислот, причем получают смесь N-алкил- и диалкиланилинов:
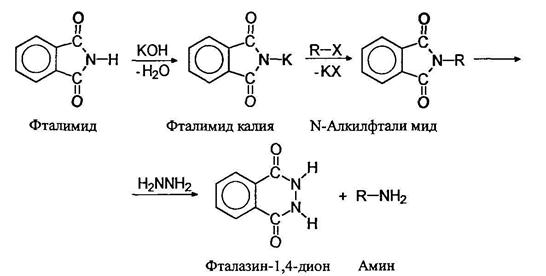
Фталимидный метод Габриэля. Аммонолиз алкилгалогенидов и алкилирование аммика спиртами приводят к образованию смесей аминов, разделение которых представляет большую трудность. Индивидуальные первичные амины можно получать фталимидным методом Габриэля:
Восстановление алкилазидов Восстановление алкилазидов, получаемых взаимодействием алкилгалогенидов с азидом натрия также приводит к образованию индивидуальных первичных аминов:
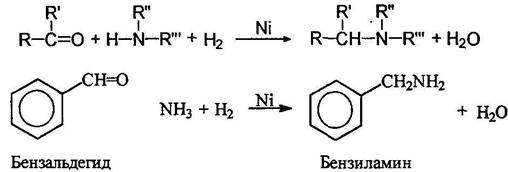
Восстановительное аминирование альдегидов и кетонов Многие альдегиды и кетоны превращаются в амины при нагревании с аммиаком и водородом в присутствии катализатора гидрирования:
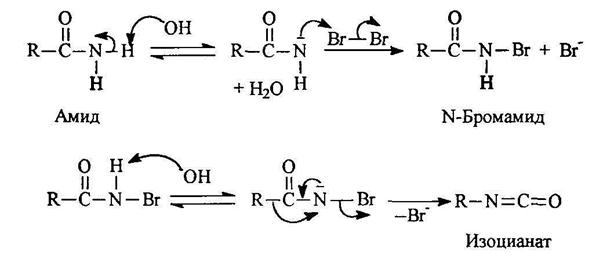
Расщепление амидов по Гофману Реакция проходит по следующему механизму:
Первичные амины могут быть получены при действии на амиды брома в щелочной среде:
Нитрилы при действии восстановителей или водорода в присутствии катализаторов превращаются в первичные амины:
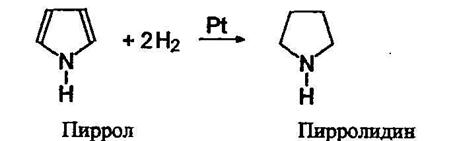
При гидрировании пиррола образуется пирролидин;
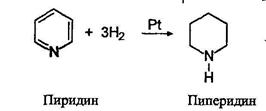
Пиридин восстанавливается водородом в момент выделения в пиперидин:
Реакции аминовАлкилирование алкилгалогенидами (реакция Меншуткина) Амины бурно реагируют с алкилгалогенидами, образуя смеси аминов и солей четвертичных аммониевых оснований:
Соли четвертичных аммониевых оснований переводят в щелочной среде в сами основания. Последние можно выделить, обрабатывая соль четвертичного аммониевого основания влажным оксидом серебра:
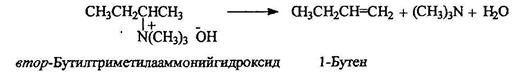
Термическое разложение четвертичных аммониевых оснований (по Гофману) приводит к образованию алкенов с крайним расположением двойной связи:
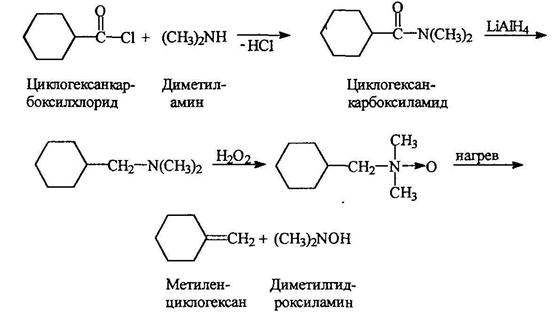
Окисление Третичные амины могут быть окислены пероксидом вродорода или надкислотами в N-оксиды:
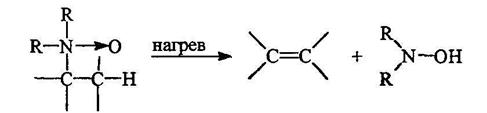
Реакция проводится в метаноле при обычной температуре. При нагревании N-оксиды расщепляются с образованием алкена и дизамещенного гидроксиламина:
При этом метильные группы при атоме азота не затрагиваются. Этим пользуются при получении алкенов определенного строения (реакция Коупа):
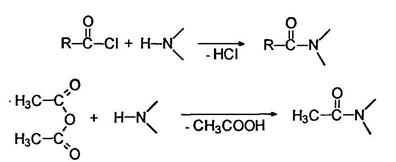
Ацилирование Подобно аммиаку первичные и вторичные амины реагируют с ацильными соединениями:
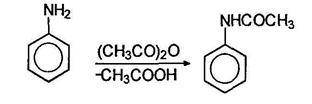
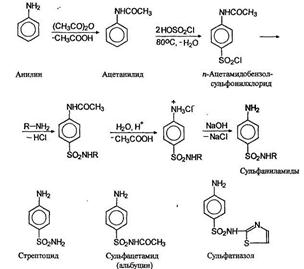
Так, при действии на анилин уксусного ангидрида образуется ацетанилид:
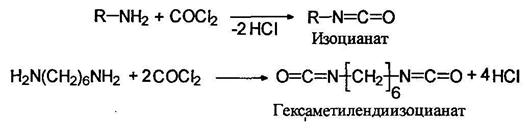
Изоцианаты При действием на первичные амины фосгена (фосгенирование) образуются изоцианаты:
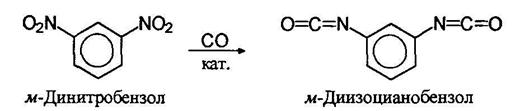
В последнее время изоцианаты стали получать действием на нитро со единения окиси углерода в присутствии катализатора:
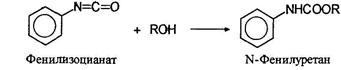
При взаимодействии изоцианатов со спиртами образуются карбаматы или уретаны:
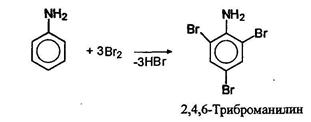
Образование шиффовых оснований При слабом нагревании ароматических первичных аминов с ароматическими альдегидами легко получаются так называемые основания Шиффа. В такую же реакцию первичные амины вступают не только с альдегидами, но и с некоторыми кетонами. Общее название образующихся продуктов - азометины. При действии разбавленных кислот азометины подвергаются гидролизу. Замещение ароматических аминов в кольцо Амино и алкиламиногруппы -NH2, -NHR и -NR являются сильными ориентантами первого рода. Активация бензольного кольца аминогруппой столь велика, что при галогенировании ароматических аминов атомы галогенов стремятся занять все орто- и пара-положения:
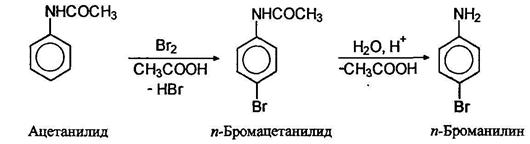
Ацетамидогруппа -NHCOCH3 также является ориентантом первого рода, хотя и более слабым, чем аминогруппы. Один атом галогена можно ввести, если аминогруппу предварительно проацилировать, а затем снять ацильную группу гидролизом:
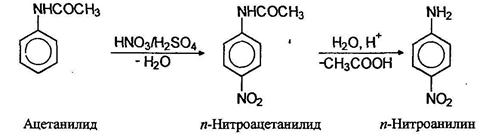
Нитрование аминов сопровождается их окислением, поэтому перед нитрованием аминогруппу защищают, переводя ее в амидную группу, полученный нитроамид далее гидролизуют в нитроамин:
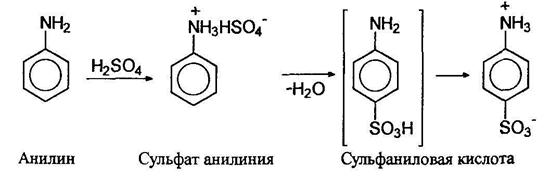
Молекула сульфаниловой кислоты включает и основание, и кислоту, и поэтому она существует в виде диполярного иона (цвиттериона). Сульфаниловая кислота имеет большое значение как элемент структуры сульфамидных препаратов, являющихся производными амида сульфаниловой кислоты (сульфаниламида). Их получают по схеме:
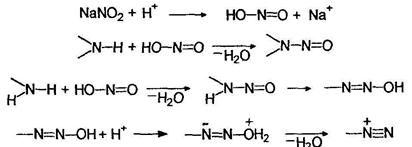
Взаимодействие аминов с азотистой кислотой Азотистая кислота сама по себе при обычной температуре неустойчива, поэтому ее генерируют в момент проведения реакции из солей:
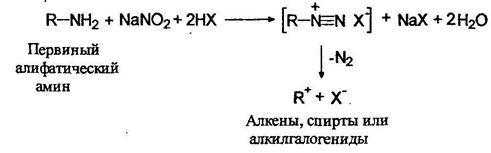
Первичные (1°), вторичные (2 °) и третичные (3°) амины как жирного, так и ароматического рядов различаются по своему поведению в реакциях с азотистой кислотой. Первичные алифатические амины реагируют с азотистой кислотой с образованием совершенно неустойчивых солей диазония, разлагающихся с выделением азота и образованием карбокатионов:
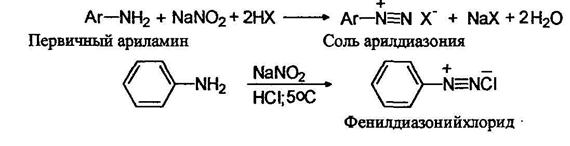
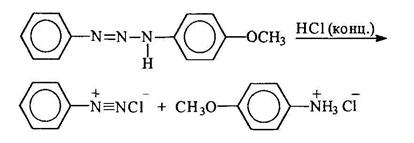
Первичные ароматические амины реагируют с азотистой кислотой с образованием относительно устойчивых солей диазония:
Названия солей диазония образуются путем добавления окончания диазоний к названию арильного радикала с указанием названия аниона. При взаимодействии вторичных алифатических и ароматических аминов с азотистой кислотой реакция останавливается на стадии образования нитрозоминов:
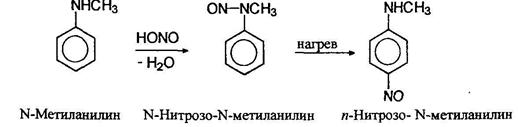
При нагревании ароматических нитрозоаминов они изомеризуются с переходом нитрозогруппы от азота к кольцу (перегруппировка Фишера-Хеппа):
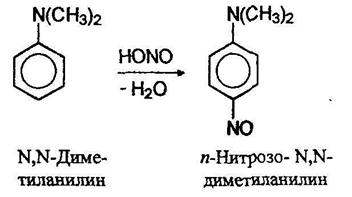
Третичные алифатические амины на холоде образуют с азотистой кислотой соли. Третичные жирноароматические амины при действии азотистой кислоты претерпевают реакцию замещения в кольцо с образованием окрашенных в зеленый цвет нитрозоариламинов:
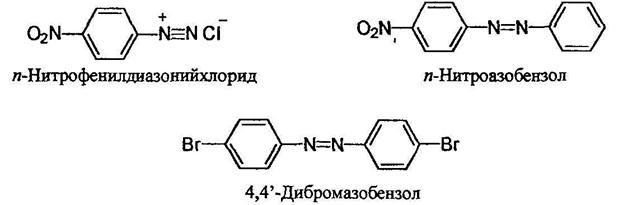
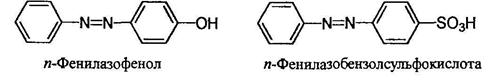
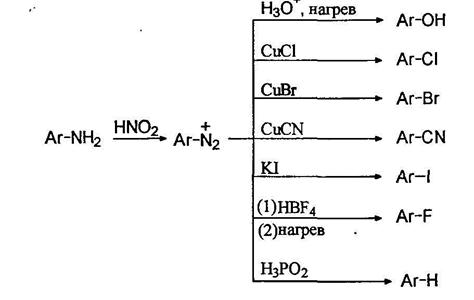
Диазо- и азосоединенияОрганические соединения, содержащие в молекуле два атома азота, связанные кратной связью и не входящие в циклическую систему, могут относиться как к азо-, так и диазо соединениям. В случае диазосоединений два атома азота соединены лишь с одним углеводородным радикалом Ar-N2+Cr, а в случае азосоединений - с двумя Ar-N=N-Ar Азосоединения интенсивно окрашены. В зависимости от структуры молекулы они могут быть окрашены в интенсивно желтый, оранжевый, красный, синий или даже зеленый цвет. Примерно половина используемых в настоящее время красителей являются азокрасителями. Диазосо единения называют как соли арилдиазониев. Азосоединения называют двумя путями - как производные азобензола;
Более сложные соединения называют, рассматривая арилазогруппу Ar-N=N- как заместитель:
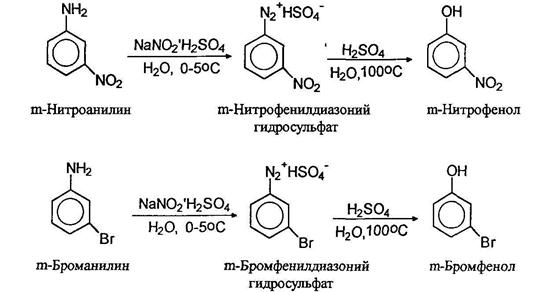
Реакции солей арилдиазонияВсе реакции солей арилдиазониев можно разделить на две группы: реакции с выделением азота и реакции без выделения азота. Реакции замещения Диазогруппа может быть замещена на разнообразные группы, это является одним из самых лучших путей введения функциональных групп в ароматическое ядро:
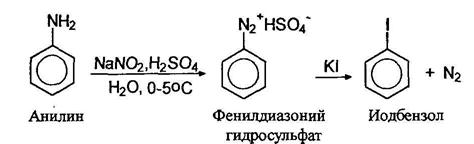
При нагревании водных растворов сульфатов диазониев происходит отщепление азота и образуются фенолы. Таким образом можно получать фенолы с различными заместителями в ароматическом кольце, например:
Соли арилдиазониев реагируют с иодидами натрия или калия образуя арилиодиды:
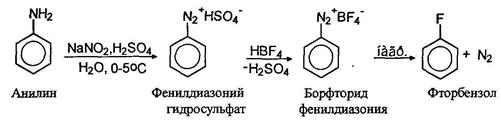
Для замещения диазогруппы на фтор к раствору соли диазония прибавляют тетрафторборную кислоту, при этом осаждается борфториды диазония, которые отфильтровывают, промывают и сушат. При осторожном нагревании борфториды диазония разлагаются с образованием арилфторидов:
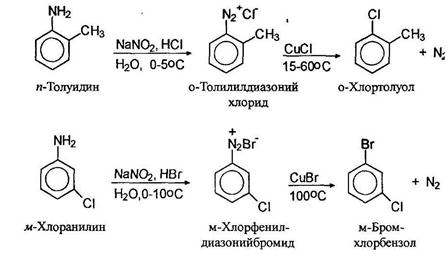
Замещение диазогруппы на хлор и бром осуществляется действием на свежеприготовленный раствор соли диазония хлоридом или бромидом одновалентной меди. Считают, что реакция проходит по радикальному механизму (реакция Зандмеера):
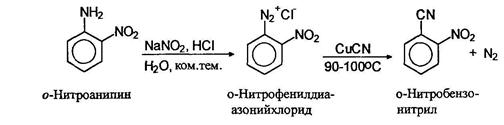
Замещение диазогруппы на нитрильную осуществляется также по реакции Зандмеера использованием цианида одновалентной меди.
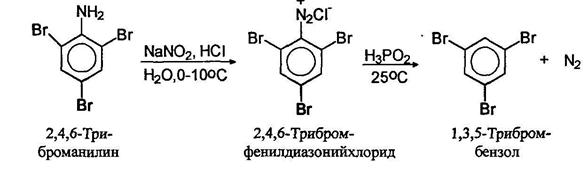
Вместо солей меди (I) в качестве катализатора можно использовать свежеосажденную порошкообразную металлическую медь. Азосочетание Замещение диазогруппы на водород можно осуществлять с помощью нескольких реагентов. Наиболее широкое применение получила фосфорноватистая (гипофосфористая) кислота. Соли диазония просто оставляют стоять в присутствии фосфорноватистой кислоты. С помощью этой оеакпии удаляют аминогруппу с ароматического кольца.
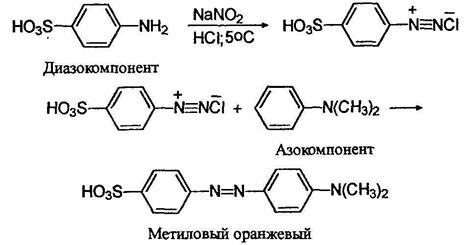
Азосочетанием получают красители. Окрашенные вещества поглощают из падающего на них видимого света некоторые лучи и отражают все остальные - цвет отраженных лучей и определяет окраску вещества. Чем длиннее цепь сопряжения, тем глубже окраска вещества. Согласно одной из теорий цветности, окрашенное соединение должно содержать так называемую хромофорную группировку - это может быть, например, пара атомов соединенных двойной связью: ОС, C=N, N=N. Очень полезно присутствие в молекуле так называемой ауксохромной группировки, несущей одну или несколько подвижных электронных пар: при ее наличии цвет вещества углубляется. Пример такой групприровки диметиламиногруппа - N(CH3)2- Вот, к примеру, краситель метиловый оранжевый, очень широко применяемый как индикатор на кислоты. Его получают из сульфаниловой кислоты и К,К-диметиланилина:
В молекуле этого красителя присутствует хромофорная двойная азот-азотная связь и ауксохромная диметиламиногруппа.
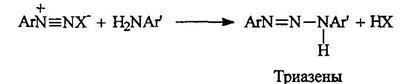
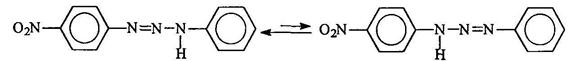
Триазены существуют в двух таутомерных формах: В средах, близких к нейтральной, катионы диазония электрофильно атакуют неподеленную пару электронов азота первичной аминогруппы. Образующиеся при этом аминоазосоединения называют триазенами.
Равновесие смещено в сторону образования триазена, в молекуле которого протон находится у более основного атома азота, т. е. связанного с более электронодонорным радикалом:
При действии минеральных кислот триазены расщепляются. При этом если триазен несимметричный, расщепление происходит таким образом, что отщепляется амин, являющийся более сильным основанием, а из "азофрагмента" образуется соответствующая соль диазония:
Список литературы 1. "Справочник химика" т.2, Л.-М.: Химия, 1964 стр. 418-419. 2. Бандман А.Л., Волкова Н.В. и др. Вредные химические вещества. Неорганические соединения элементов V–VIII групп. Справочное издание. Под ред. В.А.Филова и др. Л.: Химия, 1989, 592 с 3. Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. – М.: Высш. шк., 1973. - 623 с. 4. Препаративная органическая химия. Изд. 2-е, М., Госхимиздат, 1964. 5. Мельниченко Г.Ф., Кирсанова В.Ф., Биткова Н.П. Выращивание экологически чистой овощной продукции: томаты, перец, баклажаны. Благовещенск, 1993, 62. 6. Богословский Б.Н., Щитова Э.П. Опыты по химии с экологической направленностью. Благовещенск, 1993, 27 с.. 7. Терней А. Современная органическая химия: В 2 т. - М.: Мир, 1981. - Т.1 - 670 с; Т.2 - 615 с. 8. В. Ф. Травень. Органическая химия. Том 1. – М.: Академкнига, 2004, - 708 с. |
|
|
| 17.06.2012 |
| Большое обновление Большой Научной Библиотеки |
| 12.06.2012 |
| Конкурс в самом разгаре не пропустите Новости |
| 08.06.2012 |
| Мы проводим опрос, а также небольшой конкурс |
| 05.06.2012 |
| Сена дизайна и структуры сайта научной библиотеки |
| 04.06.2012 |
| Переезд на новый хостинг |
| 30.05.2012 |
| Работа над улучшением структуры сайта научной библиотеки |
| 27.05.2012 |
| Работа над новым дизайном сайта библиотеки |